Tìm hiểu phương pháp Giảm cân
Biến chứng của đái tháo đường
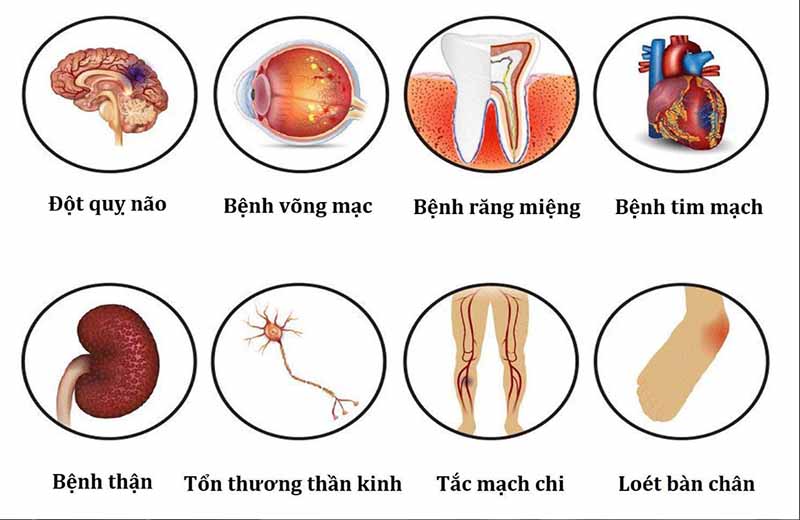
Bệnh nhân đái tháo đường (DM), nhiều năm kiểm soát đường huyết kém dẫn đến nhiều biến chứng, chủ yếu mạch máu, ảnh hưởng mạch máu nhỏ (vi mạch), mạch máu lớn (mạch máu lớn), hoặc cả hai.
Các cơ chế phát triển bệnh mạch máu gồm
-
Glycosyl hóa của protein huyết thanh và mô với sự hình thành sản phẩm cuối của sự glycosyl hóa.
-
Sản phẩm Superoxide
-
Protein kinase C hoạt tính, một phân tử báo hiệu làm tăng khả năng thẩm thấu mạch máu và gây rối loạn chức năng nội mô
-
Con đường sinh tổng hợp hexosamine và polyol được tăng tốc dẫn đến sự tích tụ sorbitol trong các mô
-
Tăng huyết áp và rối loạn lipid máu thường đi kèm với bệnh đái tháo đường
-
Vi huyết khối động mạch
-
Ảnh hưởng tiền viên và đông máu của tăng đường huyết và tăng insulin làm suy giảm tự điều hòa mạch máu
Bệnh vi mạch tiềm ẩn 3 tổn thương phổ biến và phá hủy của đái tháo đường:
Bệnh vi mạch cũng có thể giảm liền da, thậm chí tổn thương nhỏ trên da lành có thể phát triển thành loét sâu hơn và dễ bị nhiễm khuẩn, đặc biệt ở chi dưới. Kiểm soát glucose huyết tương tích cực có thể phòng tránh hoặc làm chậm nhiều biến chứng này nhưng không thể đảo ngược một khi biến chứng đã hình thành.
Bệnh mạch máu lớn liên quan xơ vữa động mạch của các mạch lớn, có thể dẫn tới
Rối loạn chức năng miễn dịch là một biến chứng lớn khác và phát triển từ những tác động trực tiếp của tăng đường huyết trên miễn dịch tế bào. Bệnh nhân đái tháo đường đặc biệt dễ bị nhiễm trùng do vi khuẩn và do nấm.
Bệnh võng mạc đái tháo đường
Bệnh võng mạc do tiểu đường là nguyên nhân phổ biến gây mù lòa ở người trưởng thành ở Hoa Kỳ. Bệnh được đặc trưng ban đầu bởi vi phình mạch của mao mạch võng mạc (nền tảng bệnh võng mạc) và sau đó là tân sinh mạch máu (bệnh võng mạc tăng sinh) và phù hoàng điểm. Không có triệu chứng ban đầu, nhưng mờ khu trú, bong thủy tinh thể hoặc võng mạc và mất thị lực một phần hoặc toàn bộ cuối cùng có thể phát triển; tốc độ tiến triển rất khác nhau.
Sàng lọc và chẩn đoán bằng cách khám võng mạc do bác sĩ nhãn khoa thực hiện, nên được thực hiện thường xuyên (thường là hàng năm) ở cả bệnh tiểu đường loại 1 và loại 2. Phát hiện sớm và điều trị là rất quan trọng để ngăn ngừa mất thị lực. Điều trị cho tất cả bệnh nhân bao gồm kiểm soát tích cự đường huyết và huyết áp. Quang đông bằng laser qua ống tủy được sử dụng cho bệnh võng mạc tiểu đường tăng sinh và đôi khi bệnh võng mạc nặng không tăng sinh do tiểu đường. Thuốc ức chế yếu tố tăng trưởng nội mô mạch máu (VEGF) như aflibercept, bevacizumab và ranibizumab được sử dụng cho phù hoàng điểm và cũng có thể được sử dụng cho bệnh võng mạc tăng sinh, nhưng điều trị này đòi hỏi phải thăm khám thường xuyên.
Bệnh thận đái tháo đường
Bệnh thận do tiểu đường là nguyên nhân hàng đầu gây ra bệnh thận mạn tính ở Hoa Kỳ. Bệnh được đặc trưng bởi sự dày lên của màng đáy cầu thận, tăng sinh gian mạch, và xơ cứng cầu thận. Những thay đổi này gây tăng huyết áp cầu thận và giảm dần mức lọc cầu thận (GFR). Tăng huyết áp toàn thân có thể đẩy nhanh tiến triển. Bệnh thường không có triệu chứng cho đến khi hội chứng thận hư hoặc suy thận phát triển.
Chẩn đoán bằng cách phát hiện albumin niệu hoặc giảm GFR. Khi bệnh tiểu đường được chẩn đoán (và hàng năm sau đó), cần theo dõi nồng độ albumin trong nước tiểu để có thể phát hiện sớm bệnh thận. Việc theo dõi có thể được thực hiện bằng cách đo tỷ lệ albumin:creatinine trên mẫu nước tiểu cục bộ hoặc tổng lượng albumin trong nước tiểu trong bộ sưu tập 24 tiếng. Tỷ lệ ≥ 30 mg/g ( ≥ 3,4 mg/mmol) hoặc bài tiết albumin từ 30 đến 299 mg/ngày biểu thị tăng albumin niệu vừa phải (trước đây gọi là microalbumin niệu) và bệnh thận do tiểu đường sớm. Bài tiết albumin≥ 300 mg/ngày được coi là tăng albumin niệu nghiêm trọng (trước đây gọi là albumin niệu đại thể), hoặc protein niệu rõ ràng, và biểu thị bệnh thận do tiểu đường tiến triển hơn. Thông thường, que thăm dò nước tiểu chỉ dương tính nếu lượng protein bài tiết vượt quá 300 đến 500 mg/ngày.
Điều trị là kiểm soát chặt đường huyết với kiểm soát huyết áp. Nên sử dụng thuốc ức chế men chuyển angiotensin (ACE) hoặc thuốc chẹn thụ thể angiotensin II (ARB) khi có dấu hiệu sớm nhất của albumin niệu (tỷ lệ albumin:creatinine ≥ 30 mg/g [ ≥ 3,4 mg/mmol]), để ngăn ngừa sự tiến triển của bệnh thận vì những thuốc này làm giảm huyết áp trong cầu thận và do đó có tác dụng bảo vệ thận. Tuy nhiên, những loại thuốc này chưa được chứng minh là có lợi trong phòng ngừa tiên phát (tức là ở những bệnh nhân không có albumin niệu) (1, 2, 3).
Thuốc ức chế chất đồng vận chuyển natri-glucose 2 (SGLT-2) cũng làm chậm sự tiến triển của bệnh thận và nên được kê đơn ở những bệnh nhân mắc bệnh thận do tiểu đường có mức lọc cầu thận ước tính (eGRF) ≥20 mL/phút và tỷ lệ albumin:creatinine trong nước tiểu ≥ 200 mg/g.
Fineronone, một chất đối kháng thụ thể mineralocorticoid không steroid, cũng đã được chứng minh là làm giảm nguy cơ tiến triển của bệnh thận do tiểu đường và các biến cố tim mạch và có thể được sử dụng cùng với hoặc thay thế cho thuốc ức chế ACE hoặc ARB (4).
Bệnh thần kinh đái tháo đường
Bệnh thần kinh đái tháo đường là hậu quả của thiếu máu thần kinh do bệnh vi mạch, ảnh hưởng trực tiếp của tăng đường huyết trên tế bào thần kinh, và những thay đổi trao đổi chất nội bào làm giảm chức năng thần kinh. Có nhiều dạng, gồm
-
Bệnh đa dây thần kinh đối xứng (với các biến đổi sợi nhỏ và lớn)
-
Bệnh dây thần kinh sọ não
Bệnh đa dây thần kinh đối xứng là phổ biến nhất và ảnh hưởng đến phía xa bàn chân và bàn tay (phân bố kiểu đi tất hoặc găng tay); bệnh biểu hiện như dị cảm,rối loạn cảm giác, hoặc không đau, mất cảm giác xúc giác, rung, cảm giác bản thể, hoặc nhiệt độ. Ở chi dưới, những triệu chứng này có thể dẫn đến giảm cảm nhận về chấn thương bàn chân do giày không phù hợp và mang trọng lượng bất thường, có thể dẫn đến loét chân và nhiễm trùng hoặc gãy xương, sai khớp, và trật khớp hoặc phá hủy cấu trúc bàn chân bình thường (bệnh khớp Charcot). Bệnh thần kinh sợi nhỏ được đặc trưng bởi cảm giác đau, tê và mất cảm giác nhiệt độ với bảo tồn cảm giác rung và cảm giác vị trí. Bệnh nhân dễ bị loét chân và thoái hóa khớp thần kinh và có tỷ lệ mắc bệnh thần kinh tự động cao. Bệnh thần kinh sợi lớn chiếm ưu thế được đặc trưng bởi yếu cơ, mất rung và cảm giác vị trí, và giảm phản xạ gân sâu. Phổ biến tình trạng teo cơ bên trong của bàn chân và bàn chân rủ.
Bệnh thần kinh thực vật có thể gây hạ huyết áp thế đứng, không dung nạp khi gắng sức, nhịp tim nhanh khi nghỉ, khó nuốt, buồn nôn và nôn (do liệt dạ dày), táo bón và/hoặc tiêu chảy (bao gồm hội chứng Dumping), đại tiện không tự chủ, bí tiểu và/hoặc tiểu tiện không tự chủ, rối loạn cương dương và xuất tinh ngược và giảm khả năng bôi trơn âm đạo.
Bệnh rễ thần kinh thường ảnh hưởng đến các rễ thần kinh từ L2 đến L4, gây đau, yếu và teo chi dưới (đái tháo đường teo cơ), hoặc rễ thần kinh từ T4 đến T12, gây đau bụng (bệnh đa rễ thần kinh ngực).
Bệnh thần kinh sọ gây ra nhìn đôi, sụp mi và đồng tử không đều khi bệnh ảnh hưởng đến dây thần kinh sọ số 3 hoặc liệt vận nhãn khi bệnh ảnh hưởng đến dây thần kinh sọ số 4 hoặc số 6.
Bệnh đau đơn dây thần kinh gây ra yếu và tê ngón tay (dây thần kinh giữa) hoặc thả bàn chân (dây thần kinh peroneal). Bệnh nhân DM cũng dễ bị rối loạn chèn ép dây thần kinh, chẳng hạn như hội chứng ống cổ tay. Bệnh đau đơn dây thần kinh có thể xảy ra đồng thời ở một số nơi (viêm đa dây thần kinh). Tất cả có xu hướng ảnh hưởng chủ yếu đến bệnh nhân lớn tuổi và thường giảm xuống trong nhiều tháng; tuy nhiên.
Chẩn đoán bệnh đa dây thần kinh đối xứng là do phát hiện giảm cảm giác và giảm phản xạ cổ chân. Mất khả năng phát hiện khi chạm nhẹ vào sợi nylon đơn giúp xác định những bệnh nhân có nguy cơ bị loét bàn chân cao nhất (xem hình Sàng lọc bàn chân do tiểu đường). Ngoài ra, rung thoa 128 Hz có thể được sử dụng để đánh giá cảm giác rung trên mu của ngón chân cái.
Các nghiên cứu về điện cơ và dẫn truyền thần kinh có thể cần thiết để đánh giá tất cả các dạng bệnh thần kinh và đôi khi được sử dụng để loại trừ các nguyên nhân khác của các triệu chứng thần kinh, chẳng hạn như bệnh cơ không do tiểu đường và hội chứng ống cổ tay.
Quản lý bệnh lý thần kinh cần một cách tiếp cận đa chiều bao gồm kiểm soát đường huyết, chăm sóc bàn chân thường xuyên và quản lý đau. Kiểm soát đường huyết chặt có thể làm giảm bệnh thần kinh. Các phương pháp điều trị để giảm triệu chứng bao gồm kem capsaicin tại chỗ, thuốc chống trầm cảm ba vòng (ví dụ: amitriptyline), thuốc ức chế tái hấp thu serotonin-norepinephrine (ví dụ: duloxetine) và thuốc chống động kinh (ví dụ: pregabalin, gabapentin). Bệnh nhân bị mất cảm giác nên kiểm tra chân hàng ngày để phát hiện chấn thương bàn chân nhỏ và ngăn chặn nó tiến triển đến nhiễm trùng nguy hiểm.
Bệnh mạch máu lớn
Xơ vữa động mạch ở mạch máu lớn là kết quả của tình trạng tăng insulin máu, rối loạn lipid máu và tăng đường huyết đặc trưng của bệnh tiểu đường. Biểu hiện là
Chẩn đoán dựa trên tiền sử và khám thực thể. Điều trị bao gồm kiểm soát chặt chẽ các yếu tố nguy cơ xơ vữa động mạch, bao gồm bình thường hóa glucose huyết tương, lipid và huyết áp, phối hợp với cai thuốc lá, uống aspirin hàng ngày (nếu có chỉ định) và nhóm statin. Một cách tiếp cận đa yếu tố bao gồm quản lý việc kiểm soát đường huyết, tăng huyết áp và rối loạn lipid máu có thể có hiệu quả trong việc giảm tỷ lệ các biến cố tim mạch. Ngược lại với bệnh vi mạch, việc kiểm soát tích cực glucose huyết tương đơn thuần đã được chứng minh là làm giảm nguy cơ mắc bệnh tiểu đường loại 1 nhưng không làm giảm nguy cơ mắc bệnh tiểu đường loại 2 (1, 2, 3). Một số loại thuốc trị tiểu đường làm giảm nguy cơ xảy ra các biến cố tim mạch nghiêm trọng, bao gồm metformin và một số thuốc ức chế SGLT2 và thuốc chủ vận thụ thể peptide-1 giống glucagon (GLP-1).
Bệnh cơ tim
Bệnh cơ tim do đái tháo đường được biết là hậu quả của nhiều yếu tố, bao gồm xơ vữa động mạch màng ngoài tim, tăng huyết áp và phì đại thất trái, bệnh vi mạch, rối loạn chức năng nội mạc và rối loạn chức năng thần kinh tự chủ, béo phì và rối loạn chuyển hóa. Bệnh nhân bị suy tim do suy giảm chức năng tâm thu và tâm trương thất trái và có nhiều khả năng phát triển suy tim sau nhồi máu cơ tim.
Nhiễm trùng
Bệnh nhân bị bệnh tiểu đường được kiểm soát kém dễ bị nhiễm trùng do vi khuẩn và nấm do tác dụng bất lợi của tăng đường huyết đối với chức năng của bạch cầu hạt và tế bào T. Ngoài việc tăng nguy cơ mắc các bệnh truyền nhiễm, những người mắc bệnh tiểu đường còn dễ bị nhiễm nấm da niêm mạc (ví dụ: nhiễm nấm candida ở miệng và âm đạo) và nhiễm trùng bàn chân do vi khuẩn (bao gồm viêm tủy xương), thường trầm trọng hơn do suy mạch máu chi dưới và bệnh thần kinh do tiểu đường. Tăng đường huyết là một yếu tố nguy cơ đã được xác định cho các trường hợp nhiễm trùng phẫu thuật.
Những người mắc bệnh tiểu đường có nguy cơ cao hơn bị bệnh nặng hoặc tử vong do COVID-19; bệnh tiểu đường loại 1 hoặc bệnh tiểu đường loại 2 đều là yếu tố nguy cơ độc lập dẫn đến tử vong liên quan đến COVID (1). Ở những người mắc bệnh tiểu đường bị nhiễm SARS-CoV-2, nồng độ đường trong máu cao hơn có liên quan đến kết quả kém hơn, bao gồm cả tỷ lệ tử vong cao hơn. Một số nghiên cứu đã báo cáo nguy cơ mắc bệnh tiểu đường loại 1 mới khởi phát tăng lên liên quan đến COVID-19 (2); tuy nhiên, các nghiên cứu khác cho thấy tác động này có thể là do sự chậm trễ trong chẩn đoán do lệnh phong tỏa của đại dịch.
Bệnh gan nhiễm mỡ liên quan đến rối loạn chuyển hóa (MASLD)
Bệnh gan do nhiễm mỡ liên quan đến chuyển hóa (MASLD, trước đây là bệnh gan nhiễm mỡ không do rượu [NAFLD]), ngày càng phổ biến và là một bệnh đi kèm quan trọng của bệnh tiểu đường loại 2. Một số nghiên cứu đã phát hiện ra rằng hơn một nửa số bệnh nhân mắc bệnh tiểu đường loại 2 bị MASLD (1). MASLD cũng có thể xảy ra ở những bệnh nhân mắc hội chứng chuyển hóa, béo phì và rối loạn lipid máu mà không bị đái tháo đường.
Chẩn đoán MASLD cần có bằng chứng về tình trạng nhiễm mỡ ở gan bằng hình ảnh hoặc mô học và không có các nguyên nhân gây tích tụ mỡ khác (chẳng hạn như uống rượu hoặc thuốc gây tích tụ mỡ) (2). MASLD xảy ra khi có ≥ 5% gan nhiễm mỡ nhưng không có bằng chứng tổn thương tế bào gan. Ngược lại, viêm gan nhiễm mỡ liên quan đến rối loạn chức năng chuyển hóa (MASH), trước đây là viêm gan nhiễm mỡ không do rượu (NASH), đòi hỏi cả gan nhiễm mỡ (≥ 5%) và viêm kèm tổn thương tế bào gan. Xơ hóa cũng có thể xảy ra trong MASH và có thể dẫn đến xơ gan. Cơ chế bệnh sinh của MASLD chưa được hiểu rõ nhưng rõ ràng có liên quan đến tình trạng kháng insulin, dẫn đến tích tụ triglycerides trong gan.
Những người mắc bệnh tiểu đường loại 2 có thể được sàng lọc bệnh xơ hóa bằng cách tính chỉ số xơ hóa 4 cho bệnh xơ gan (chỉ số FIB-4) theo tuổi, mức độ aminotransferase và số lượng tiểu cầu. Có thể thực hiện thêm các xét nghiệm khác để tìm kiếm tình trạng xơ hóa, bằng đo độ đàn hồi thoáng qua hoặc các chất chỉ điểm xơ hóa trong máu nếu điểm FIB-4 cho thấy nguy cơ xơ hóa không xác định hoặc cao.
Điểm chính của điều trị là chế độ ăn uống, tập luyện và giảm cân. Ở những bệnh nhân mắc bệnh tiểu đường và có bằng chứng MASH, việc sử dụng pioglitazone hoặc thuốc chủ vận thụ thể GLP-1 như là liraglutide hoặc semaglutide đã được chứng minh là làm chậm sự tiến triển của xơ hóa (3, 4, 5, 6, 7). Có thể sử dụng các loại thuốc khác có tác dụng giảm cân ở bệnh nhân tiểu đường (ví dụ: polypeptide insulinotropic kép phụ thuộc glucose [GIP] và thuốc ức chế GLP-1 tirzepatide, thuốc ức chế SGLT-2).
Biến chứng khác của đái tháo đường
Biến chứng bàn chân đái tháo đường (thay đổi da, loét, nhiễm trùng, hoại tử) là phổ biến và có thể do bệnh mạch máu, thần kinh, và liên quan tới ức chế miễn dịch. Những biến chứng này có thể dẫn đến cắt cụt chi dưới.
Chắc chắn rối loạn cơ xương phổ biến hơn ở bệnh nhân tiểu đường, bao gồm cả nhồi máu cơ, Hội chứng ống cổ tay, Hợp đồng Dupuytren, viêm bao quy đầu dính, và sclerodactyly.
Bệnh nhân tiểu đường cũng có thể phát triển
-
Bệnh nhãn khoa không liên quan đến bệnh võng mạc do tiểu đường (ví dụ: đục thủy tinh thể, tăng nhãn áp, trợt giác mạc, bệnh thần kinh thị giác)
-
Bệnh da liễu (ví dụ: nhiễm trùng nấm da, loét chi dưới, bệnh da do đái tháo đường, bệnh đái tháo đường lipoidica hoại tử, bệnh xơ cứng hệ thống do đái tháo đường, bạch biến, u hạt tiêu, acanthosis nigricans [một dấu hiệu của insulin Sức cản])
