Tìm hiểu phương pháp Giảm cân
U tuỷ thượng thận
/https://cms-prod.s3-sgn09.fptcloud.com/u_tuy_thuong_than_1_72ec02c0b1.jpg)
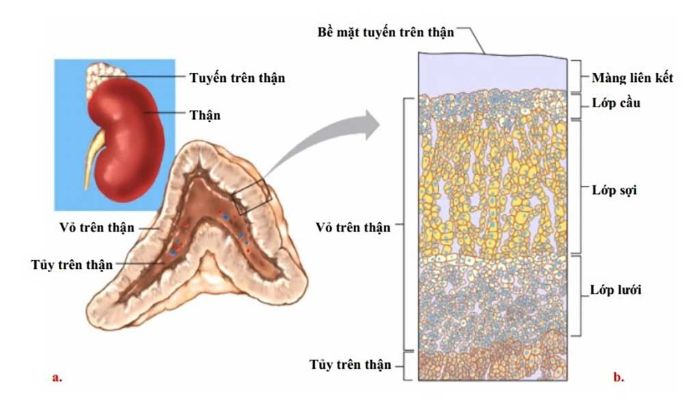
U tủy thượng thận là một khối u giải phóng catecholamine của các tế bào ưa crôm nằm ở thượng thận. Nó gây tăng huyết áp dai dẳng hoặc tăng huyết áp kịch phát. Chẩn đoán là bằng cách đo các sản phẩm catecholamine trong máu hoặc nước tiểu. Chẩn đoán hình ảnh, đặc biệt là CT hoặc MRI, giúp xác định khối u. Điều trị bao gồm đến việc cắt bỏ khối u khi có thể. Thuốc chẹn alpha, thường phối hợp với thuốc chẹn beta, được sử dụng để kiểm soát huyết áp.
Các catecholamine được tiết ra bao gồm norepinephrine, epinephrine, dopamine, và dopa với các tỷ lệ khác nhau.
Hầu hết u tế bào ưa crôm nằm trong
-
Tủy thượng thận (khoảng 90%)
U tế bào ưa crôm cũng có thể nằm trong các mô khác có nguồn gốc từ tế bào mào thần kinh. Các vị trí có thể có bao gồm:
-
hạch giao cảm
-
hạch sau phúc mạc quanh động mạch chủ
-
Thân động mạch cảnh
-
Organ của Zuckerkandl (tại sự phân chia động mạch chủ)
-
Hệ tiết niệu sinh dục
-
Não
-
Bao màng ngoài tim
-
u nang dạng bì
U tế bào ưa crôm ở tủy thượng thận xảy ra như nhau ở cả hai giới, ở hai bên trong 10% trường hợp (20% ở trẻ em) và ác tính ở < 10% (1). Trong số các u tế bào ưa crom ngoài tuyến thượng thận (được gọi là u cận hạch), 30% là ác tính. Mặc dù u tế bào ưa crôm xảy ra ở mọi lứa tuổi, tỷ lệ mắc bệnh cao nhất là từ 20 tuổi đến 40 tuổi. Gần 50% được cho là do đột biến dòng mầm. U tế bào ưa crom ngoài tuyến thượng thận có nhiều khả năng là ác tính và di căn.
U tủy thượng thận có kích thước khác nhau nhưng đường kính trung bình từ 5 đến 6 cm. Mỗi khối u có trọng lượng từ 50 đến 200 g, nhưng cũng có nhiều khối u nặng hơn vài kilogram đã được báo cáo. Hiếm khi, khối u có thể đủ lớn để có thể sờ thấy hoặc gây ra các triệu chứng do chèn ép hoặc tắc nghẽn. Bất kể hình thái mô học, khối u được coi là lành tính nếu nó không xâm chiếm vỏ bao tuyến và không có di căn, mặc dù ngoại lệ có thể vẫn xảy ra. Nhìn chung, các khối u lớn hơn có nhiều khả năng tái phát hoặc di căn hơn.
U tế bào ưa crôm có thể là một phần của hội chứng đa u nội tiết gia đình (MEN) loại 2A và 2B, trong đó các khối u nội tiết khác (ung thư biểu mô tuyến cận giáp hoặc ung thư biểu mô tủy tuyến giáp) cùng tồn tại hoặc phát triển sau đó. U tế bào ưa crom phát triển ở 1% bệnh nhân với bệnh u xơ thần kinh và có thể xảy ra với u nguyên bào mạch máu và ung thư biểu mô tế bào thận, như trong bệnh von Hippel-Lindau. U pheochromocytomas và khối u cơ thể động mạch cảnh có thể do đột biến gen mã hóa enzym succinate dehydrogenase hoặc các phân tử tín hiệu khác.
U cận hạch phát sinh ở đầu hoặc cổ có nguồn gốc từ các tế bào chromaffin trong hạch phó giao cảm, có thể tiết ra catecholamine và được gọi là u cận hạch đầu và cổ.
Triệu chứng và Dấu hiệu u tủy thượng thận
Tăng huyết áp kịch phát ở 45% số bệnh nhân, xảy ra ở hầu hết bệnh nhân có u tế bào ưa crôm và nổi bật. Ngược lại, khoảng 0,2% đến 0,6% số bệnh nhân tăng huyết áp có u tủy thượng thận (1). Các triệu chứng và dấu hiệu phổ biến là
-
Nhịp tim nhanh
-
Ra mồ hôi
-
Hạ huyết áp tư thế
-
Thở nhanh

-
Da lạnh và ẩm
-
Đau đầu nặng
-
Đau thắt ngực
-
Đánh trống ngực
-
Buồn nôn và nôn

-
Đau vùng thượng vị
-
Rối loạn thị giác
-
Khó thở
-
Dị cảm
-
Táo bón
-
Một cảm giác về tai họa sắp tới
Cơn kịch phát có thể kích thích bởi va chạm khối u, thay đổi tư thế, bóp bụng hoặc xoa bóp, gây mê, chấn thương tâm lý, không dùng thuốc ức chế beta (đối lập tăng huyết áp bằng cách ức chế beta giãn mạch trung gian), hoặc tiểu tiện (nếu khối u là trong bàng quang). Ở những bệnh nhân cao tuổi, giảm cân nghiêm trọng kèm theo cao huyết áp kéo dài gợi ý bệnh u tủy thượng thận.
Khám thực thể, ngoại trừ sự có mặt của cao huyết áp, thường là bình thường trừ khi được thực hiện trong cơn kịch phát. Bệnh võng mạc và chứng tim to thường ít nghiêm trọng hơn mức có thể xảy ra đối với mức độ cao huyết áp, nhưng có thể xảy ra bệnh cơ tim catecholamine đặc hiệu. Tuy nhiên, các biến cố về tim và mạch máu não thường gặp hơn ở những bệnh nhân mắc u tế bào ưa crôm so với những người khác có mức huyết áp tương tự.
Điều trị u tủy thượng thận
-
Kiểm soát huyết áp với sự kết hợp giữa các thuốc chẹn alpha và thuốc chẹn beta
-
Phẫu thuật cắt bỏ khối u với việc kiểm soát huyết áp cẩn thận và tình trạng thể tích
Phẫu thuật loại bỏ khối u là sự lựa chọn của điều trị. Hoạt động thường được trì hoãn cho đến khi tăng huyết áp được kiểm soát bằng sự kết hợp của thuốc chẹn alpha và thuốc chẹn beta (thường là phenoxybenzamine 20 đến 40 mg uống 3 lần một ngày và propranolol 20 đến 40 mg uống 3 lần một ngày).
Mục tiêu huyết áp là < 130/80 mmHg; một số ý kiến cho rằng mục tiêu này cũng cần phải bao gồm việc hạ huyết áp theo tư thế nhất định, nhưng điều này không cần thiết. Việc tái cân bằng hệ thống tim mạch cần khoảng 10 ngày đến 14 ngày, sau đó tác dụng chặn được cho là có hiệu quả. Không nên dùng thuốc chẹn beta khi dùng alpha có hiệu quả. Một số thuốc chẹn alpha, chẳng hạn như doxazosin, có thể có hiệu quả tương đương nhưng dung nạp tốt hơn.
Nitroprusside có thể được truyền vào các cơn cao huyết áp trong thời gian trước hoặc trong mổ.
Khi ghi nhận hoặc nghi ngờ có khối u hai bên (như ở bệnh nhân mắc bệnh đa u nội tiết [MEN]), dùng đủ hydrocortisone (100 mg đường tĩnh mạch hai lần mỗi ngày) trước và trong khi phẫu thuật sẽ tránh được tình trạng thiếu glucocorticoid cấp tính do cắt bỏ tuyến thượng thận hai bên. Đôi khi phẫu thuật bảo tồn phần vỏ là một giải pháp thay thế.
Hầu hết các khối u tế bào ưa crom có thể được cắt bỏ bằng nội soi ổ bụng. Tăng huyết áp phải được theo dõi liên tục thông qua một carthete trong động mạch, và tình trạng thể tích được theo dõi chặt chẽ. Nên gây mê bằng thuốc không gây rối loạn nhịp tim và tiếp tục bằng thuốc hít (ví dụ: enflurane, isoflurane). Trong khi phẫu thuật, nên kiểm soát các cơn tăng huyết áp kịch phát bằng cách tiêm phentolamine 1 đến 5 mg theo đường tĩnh mạch hoặc truyền nitroprusside (2 đến 4 mcg/kg/phút) và nên kiểm soát loạn nhịp nhanh bằng propranolol hoặc esmolol. Nếu cần phải làm giãn cơ, thuốc ức chế giải phóng histamin được ưa thích dùng. Không nên dùng atropine trước phẫu thuật.
Trước khi khối u được cắt bỏ, có thể phải truyền máu trước khi phẫu thuật (1 đến 2 đơn vị). Nếu huyết áp đã được kiểm soát tốt trước khi phẫu thuật, nên áp dụng chế độ ăn nhiều muối để tăng lượng máu. Có thể cân nhắc truyền norepinephrine từ 4 đến 12 mg/L trong dung dịch chứa dextrose bắt đầu từ 0,05 mcg/kg/phút và chuẩn độ liều để có tác dụng nếu bị tụt huyết áp. Một số bệnh nhân bị hạ huyết áp đáp ứng kém norepinephrine có thể có thể dùng hydrocortisone 100 mg IV, nhưng việc thay thế chất lỏng phù hợp thường là tất cả những gì được yêu cầu.
U tế bào ưa crom ác tính di căn ác tính nên được điều trị bằng thuốc chẹn alpha- và beta-blockers. Khối u có thể không đau và tồn tại lâu dài. Tuy nhiên, ngay cả khối u phát triển nhanh, huyết áp có thể vẫn được kiểm soát. I-131-MIBG hoặc gần đây là lutetium-177 dotatate có thể giúp làm giảm các triệu chứng ở bệnh nhân mắc bệnh còn sót lại. Metrosine, một chất ức chế hydroxylase tyrosine, có thể được sử dụng để giảm sản xuất catecholamine ở những bệnh nhân bị huyết áp cao khó kiểm soát. Liệu pháp xạ trị có thể làm giảm đau xương do di căn. Hóa trị hiếm khi có hiệu quả, nhưng phác đồ phổ biến nhất là dùng cyclophosphamide, vincristine và dacarbazine. Thuốc hóa trị temozolomide và liệu pháp nhắm mục tiêu bằng sunitinib hoặc có lẽ là cabozantinib cũng có thể có hiệu quả. Belzutifan, một thuốc ức chế yếu tố gây thiếu oxy được sử dụng trong điều trị các bệnh ung thư liên quan ở bệnh nhân mắc bệnh von Hippel-Lindau, hiện đang được thử nghiệm lâm sàng ở những bệnh nhân mắc u tế bào ưa crôm di căn ác tính.
